Peptidlar bir nechta aminokislotalarning peptid aloqalari orqali bog'lanishi natijasida hosil bo'lgan birikmalar sinfidir.Ular tirik organizmlarda hamma joyda uchraydi.Hozirgacha tirik organizmlarda o'n minglab peptidlar topilgan.Peptidlar turli tizimlar, organlar, to'qimalar va hujayralarning funktsional faoliyatini tartibga solishda va hayot faoliyatida muhim rol o'ynaydi va ko'pincha funktsional tahlilda, antikorlarni tadqiq qilishda, dori vositalarini ishlab chiqishda va boshqa sohalarda qo'llaniladi.Biotexnologiya va peptid sintez texnologiyasining rivojlanishi bilan ko'proq peptid preparatlari ishlab chiqildi va klinikada qo'llaniladi.
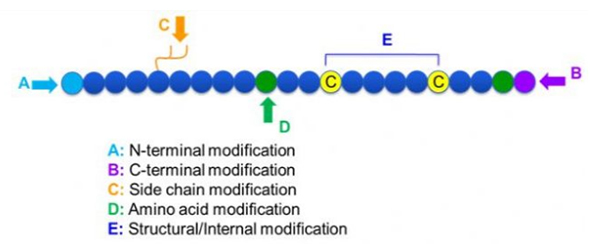
Peptid modifikatsiyalarining keng assortimenti mavjud bo'lib, ularni oddiygina post modifikatsiyasi va jarayonni o'zgartirish (olingan aminokislota modifikatsiyasi yordamida) va N-terminal modifikatsiyasi, C-terminal modifikatsiyasi, yon zanjir modifikatsiyasi, aminokislotalar modifikatsiyasi, skeletning modifikatsiyasi, o'zgartirish joyiga qarab va boshqalar (1-rasm).Asosiy zanjir tuzilishini yoki peptid zanjirlarining yon zanjir guruhlarini o'zgartirishning muhim vositasi sifatida peptid modifikatsiyasi peptid birikmalarining fizik va kimyoviy xususiyatlarini samarali o'zgartirishi, suvda eruvchanligini oshirishi, in vivo jonli ta'sir qilish vaqtini uzaytirishi, ularning biologik tarqalishini o'zgartirishi, immunogenlikni yo'q qilishi mumkin. , toksik nojo'ya ta'sirlarni kamaytirish va hokazo. Ushbu maqolada peptidlarni o'zgartirishning bir qancha asosiy strategiyalari va ularning xarakteristikalari keltirilgan.
1. Tsiklizatsiya
Tsiklik peptidlar biotibbiyotda juda ko'p qo'llaniladi va biologik faollikka ega ko'plab tabiiy peptidlar siklik peptidlardir.Tsiklik peptidlar chiziqli peptidlarga qaraganda qattiqroq bo'lganligi sababli, ular ovqat hazm qilish tizimiga juda chidamli bo'lib, ovqat hazm qilish traktida omon qolishi mumkin va maqsadli retseptorlarga nisbatan kuchliroq yaqinlikni namoyon qiladi.Tsiklizatsiya siklik peptidlarni sintez qilishning eng to'g'ridan-to'g'ri usuli hisoblanadi, ayniqsa katta strukturali skeletga ega peptidlar uchun.Tsiklizatsiya rejimiga ko'ra, u yon zanjir-yon zanjir turiga, terminal - yon zanjir turiga, terminal - terminal turiga (uchdan oxirigacha) bo'linishi mumkin.
(1) yonma-yon zanjir
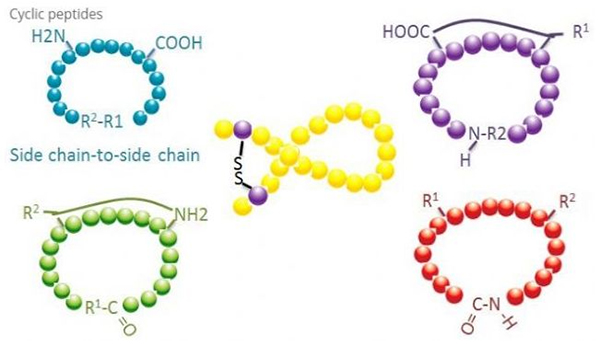
Yon zanjirdan yon zanjirga aylanishning eng keng tarqalgan turi sistein qoldiqlari orasidagi disulfid ko'prigidir.Bu sikllanish bir juft sistein qoldiqlarining himoyasizlanishi va keyin disulfid aloqalarini hosil qilish uchun oksidlanishi bilan kiritiladi.Polisiklik sintezga sulfhidril himoya guruhlarini tanlab olib tashlash orqali erishish mumkin.Tsiklizatsiya dissotsiatsiyadan keyingi erituvchida yoki dissotsiatsiyadan oldingi qatronda amalga oshirilishi mumkin.Qatronlar ustidagi siklizatsiya erituvchi siklizatsiyasidan kam samarali bo'lishi mumkin, chunki qatronlardagi peptidlar sikllangan konformatsiyalarni osonlikcha hosil qilmaydi.Yon zanjirning yana bir turi - yon zanjir siklizatsiyasi aspartik kislota yoki glutamik kislota qoldig'i va asosiy aminokislota o'rtasida amid strukturasini shakllantirish bo'lib, u yon zanjirning himoya guruhini polipeptiddan tanlab olib tashlanishini talab qiladi. qatronda yoki dissotsiatsiyadan keyin.Yon zanjirning uchinchi turi - yon zanjir siklizatsiyasi tirozin yoki p-gidroksifenilglisin ta'sirida difenil efirlarning hosil bo'lishidir.Tabiiy mahsulotlarda siklizatsiyaning bunday turi faqat mikrobial mahsulotlarda uchraydi va siklizatsiya mahsulotlari ko'pincha potentsial dorivor ahamiyatga ega.Ushbu birikmalarni tayyorlash noyob reaktsiya sharoitlarini talab qiladi, shuning uchun ular an'anaviy peptidlarni sintez qilishda tez-tez ishlatilmaydi.
(2) terminaldan yonma-yon zanjirga
Terminal yon zanjiri siklizatsiyasi odatda lizin yoki ornitin yon zanjirining aminokislotalari bilan C-terminalni yoki aspartik kislota yoki glutamik kislota yon zanjiri bilan N-terminalni o'z ichiga oladi.Boshqa polipeptid siklizatsiyasi C terminali va serin yoki treonin yon zanjirlari o'rtasida efir aloqalarini hosil qilish orqali amalga oshiriladi.
(3) Terminal yoki bosh-quyruq turi
Zanjirli polipeptidlar erituvchida aylanishi yoki yonma-yon zanjir aylanishi orqali qatronga mahkamlanishi mumkin.Peptidlarning oligomerizatsiyasini oldini olish uchun erituvchilarni markazlashtirishda peptidlarning past konsentratsiyasidan foydalanish kerak.Boshdan quyruqgacha bo'lgan sintetik halqali polipeptidning chiqishi zanjir polipeptidining ketma-ketligiga bog'liq.Shuning uchun, siklik peptidlarni keng miqyosda tayyorlashdan oldin, birinchi navbatda zanjirlangan qo'rg'oshin peptidlarining mumkin bo'lgan kutubxonasini yaratish kerak, so'ngra eng yaxshi natijalarga ega bo'lgan ketma-ketlikni topish uchun siklizatsiya qilish kerak.
2. N-metillanish
N-metilatsiya dastlab tabiiy peptidlarda paydo bo'ladi va vodorod aloqalarining shakllanishiga yo'l qo'ymaslik uchun peptid sinteziga kiritiladi va shu bilan peptidlarni biologik parchalanish va tozalashga chidamli qiladi.N-metillangan aminokislota hosilalari yordamida peptidlarni sintez qilish eng muhim usuldir.Bundan tashqari, N-(2-nitrobenzol sulfonilxlorid) polipeptid-qatronli oraliq mahsulotlarning metanol bilan Mitsunobu reaksiyasidan ham foydalanish mumkin.Ushbu usul N-metillangan aminokislotalarni o'z ichiga olgan siklik peptid kutubxonalarini tayyorlash uchun ishlatilgan.
3. Fosforlanish
Fosforlanish tabiatdagi eng keng tarqalgan post-translatsiya modifikatsiyalaridan biridir.Inson hujayralarida oqsillarning 30% dan ortig'i fosforlangan.Fosforlanish, ayniqsa teskari fosforlanish ko'plab hujayra jarayonlarini, masalan, signal o'tkazish, gen ekspressiyasi, hujayra aylanishi va sitoskeleton regulyatsiyasi va apoptozni boshqarishda muhim rol o'ynaydi.
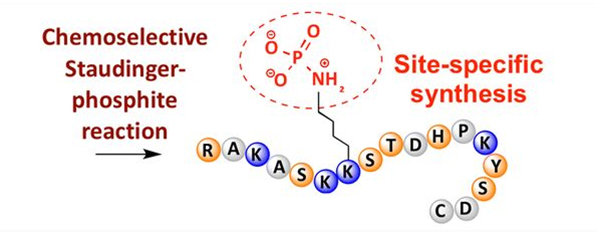
Fosforlanish turli xil aminokislotalar qoldiqlarida kuzatilishi mumkin, ammo fosforillanishning eng keng tarqalgan maqsadlari serin, treonin va tirozin qoldiqlaridir.Fosfotirozin, fosfotreonin va fosfoserin hosilalari sintez paytida peptidlarga kiritilishi yoki peptid sintezidan keyin hosil bo'lishi mumkin.Tanlangan fosforlanishga himoya guruhlarini tanlab olib tashlaydigan serin, treonin va tirozin qoldiqlari yordamida erishish mumkin.Ba'zi fosforlanish reagentlari fosfor kislotasi guruhlarini polipeptidga post modifikatsiya orqali ham kiritishi mumkin.So'nggi yillarda kimyoviy selektiv Staudinger-fosfit reaktsiyasi yordamida lizinning o'ziga xos fosforlanishiga erishildi (3-rasm).
4. Miristillanish va palmitillanish
N-terminalning yog 'kislotalari bilan asillanishi peptidlar yoki oqsillarni hujayra membranalari bilan bog'lash imkonini beradi.N-terminaldagi miridamoillangan ketma-ketlik Src oilasi protein kinazlari va teskari transkriptaza Gaq oqsillarini hujayra membranalari bilan bog'lanish uchun mo'ljallangan bo'lishiga imkon beradi.Miristik kislota standart ulanish reaktsiyalari yordamida qatron-polipeptidning N-terminaliga bog'langan va natijada olingan lipopeptid standart sharoitlarda dissotsiatsiyalanishi va RP-HPLC tomonidan tozalanishi mumkin edi.
5. Glikozillanish
Vankomitsin va teikolanin kabi glikopeptidlar dori-darmonlarga chidamli bakterial infektsiyalarni davolash uchun muhim antibiotiklardir va boshqa glikopeptidlar ko'pincha immunitet tizimini rag'batlantirish uchun ishlatiladi.Bundan tashqari, ko'plab mikrob antijenlari glikozillanganligi sababli, infektsiyaning terapevtik ta'sirini yaxshilash uchun glikopeptidlarni o'rganish katta ahamiyatga ega.Boshqa tomondan, o'simta hujayralarining hujayra membranasidagi oqsillar g'ayritabiiy glikozillanishni namoyon etishi aniqlandi, bu esa glikopeptidlarni saraton va o'sma immunitetini himoya qilish tadqiqotlarida muhim rol o'ynaydi.Glikopeptidlar Fmoc/t-Bu usulida tayyorlanadi.Treonin va serin kabi glikozillangan qoldiqlar ko'pincha glikosillangan aminokislotalarni himoya qilish uchun pentafluorofenol esteri faollashtirilgan fMOClar tomonidan polipeptidlarga kiritiladi.
6. Izopren
Izopentadienilatsiya C-terminal yaqinidagi yon zanjirdagi sistein qoldiqlarida sodir bo'ladi.Protein izopren hujayra membranasining yaqinligini yaxshilashi va oqsil-oqsil o'zaro ta'sirini shakllantirishi mumkin.Izopentadienlangan oqsillarga tirozin fosfataza, kichik GTaz, koxaperon molekulalari, yadro qatlami va sentromerik bog'lovchi oqsillar kiradi.Izopren polipeptidlarini qatronlardagi izopren yordamida yoki sistein hosilalarini kiritish orqali tayyorlash mumkin.
7. Polietilen glikol (PEG) modifikatsiyasi
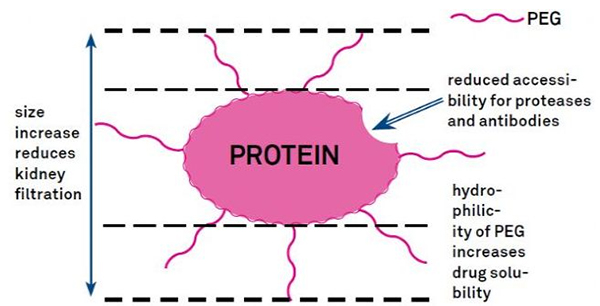
PEG modifikatsiyasi oqsil gidrolitik barqarorligini, biologik taqsimlanishini va peptid eruvchanligini yaxshilash uchun ishlatilishi mumkin.PEG zanjirlarini peptidlarga kiritish ularning farmakologik xususiyatlarini yaxshilashi va shuningdek, proteolitik fermentlar tomonidan peptidlarning gidrolizlanishini inhibe qilishi mumkin.PEG peptidlari glomerulyar kapillyar kesma orqali oddiy peptidlarga qaraganda osonroq o'tib, buyrak klirensini sezilarli darajada kamaytiradi.PEG peptidlarining in vivo jonli faol yarimparchalanish davri uzayganligi sababli, normal davolash darajasini pastroq dozalarda va kamroq tez-tez peptidli dorilar bilan ta'minlash mumkin.Biroq, PEG modifikatsiyasi ham salbiy ta'sir ko'rsatadi.Ko'p miqdorda PEG fermentning peptidni parchalanishiga to'sqinlik qiladi va peptidning maqsadli retseptorlari bilan bog'lanishini kamaytiradi.Ammo PEG peptidlarining past yaqinligi odatda ularning uzoqroq farmakokinetik yarimparchalanish davri bilan qoplanadi va organizmda uzoqroq bo'lishi bilan PEG peptidlari maqsadli to'qimalarga so'rilish ehtimoli ko'proq.Shuning uchun PEG polimer spetsifikatsiyalari optimal natijalarga erishish uchun optimallashtirilishi kerak.Boshqa tomondan, PEG peptidlari buyrak klirensining pasayishi tufayli jigarda to'planadi, natijada makromolekulyar sindrom paydo bo'ladi.Shuning uchun, peptidlar dori sinovlari uchun foydalanilganda, PEG modifikatsiyalari yanada ehtiyotkorlik bilan ishlab chiqilishi kerak.
PEG modifikatorlarining umumiy modifikatsiya guruhlarini taxminan quyidagicha umumlashtirish mumkin: Amino (-amin) -NH2, aminometil-Ch2-NH2, gidroksi-OH, karboksi-Ku, sulfgidril (-Tiol) -SH, Maleimid-MAL, suksinimid karbonat - SC, suksinimid asetat -SCM, suksinimid propionat -SPA, n-gidroksisuksinimid -NHS, akrilat-ch2ch2cooh, aldegid -CHO (masalan, propional-ald, butyrALD), akril asos (-akrilat-akrl), azido-az Biotin, flüoresan, glutaril -GA, akrilat gidrazid, alkin-alkin, p-toluensülfonat -OTs, suksinimid suksinat -SS va boshqalar. Karboksilik kislotalar bilan PEG hosilalari n-terminal aminlar yoki lizin yon zanjirlari bilan birlashtirilishi mumkin.Amino-faollashtirilgan PEG aspartik kislota yoki glutamik kislota yon zanjirlariga ulanishi mumkin.Noto'g'ri faollashtirilgan PEG to'liq himoyalanmagan sistein yon zanjirlarining merkaptaniga konjugatsiyalanishi mumkin [11].PEG modifikatorlari odatda quyidagicha tasniflanadi (eslatma: mPEG - metoksi-PEG, CH3O-(CH2CH2O)n-CH2CH2-OH):
(1) to'g'ri zanjirli PEG modifikatori
mPEG-SC, mPEG-SCM, mPEG-SPA, mPEG-OTs, mPEG-SH, mPEG-ALD, mPEG-butyrALD, mPEG-SS
(2) ikki funksiyali PEG modifikatori
HCOO-PEG-COOH, NH2-PEG-NH2, OH-PEG-COOH, OH-PEG-NH2, HCl·NH2-PEG-COOH, MAL-PEG-NHS
(3) tarmoqlanuvchi PEG modifikatori
(mPEG)2-NHS, (mPEG)2-ALD, (mPEG)2-NH2, (mPEG)2-MAL
8. Biotinizatsiya
Biotin avidin yoki streptavidin bilan kuchli bog'lanishi mumkin va bog'lanish kuchi hatto kovalent aloqaga yaqin.Biotin bilan belgilangan peptidlar odatda immunoassay, gistotsitokimyo va floresan asosidagi oqim sitometriyasida qo'llaniladi.Belgilangan antibiotik antikorlari biotinlangan peptidlarni bog'lash uchun ham ishlatilishi mumkin.Biotin yorliqlari ko'pincha lizin yon zanjiriga yoki N terminaliga biriktiriladi.6-aminokaproik kislota ko'pincha peptidlar va biotin o'rtasidagi bog'lanish sifatida ishlatiladi.Bog'lanish substrat bilan bog'lanishda moslashuvchan va sterik to'siq mavjud bo'lganda yaxshiroq bog'lanadi.
9. Floresan markalash
Floresan yorlig'i tirik hujayralardagi polipeptidlarni kuzatish va fermentlar va ta'sir mexanizmlarini o'rganish uchun ishlatilishi mumkin.Triptofan (Trp) lyuminestsentdir, shuning uchun u ichki etiketka uchun ishlatilishi mumkin.Triptofanning emissiya spektri periferik muhitga bog'liq va erituvchining polaritesining pasayishi bilan kamayadi, bu xususiyat peptid tuzilishi va retseptorlari bog'lanishini aniqlash uchun foydalidir.Triptofan floresansi protonlangan aspartik kislota va glutamik kislota bilan o'chirilishi mumkin, bu uning ishlatilishini cheklashi mumkin.Dansil xlorid guruhi (Dansyl) aminokislotalar yoki oqsillar uchun lyuminestsent yorlig'i sifatida ko'pincha aminokislotalar bilan bog'langanda yuqori floresan hisoblanadi.
Floresan-rezonans energiya konvertatsiyasi (FRET) fermentlarni o'rganish uchun foydalidir.FRET qo'llanilganda, substrat polipeptidi odatda floresan-yorliqlash guruhini va floresan-söndürme guruhini o'z ichiga oladi.Yorliqli lyuminestsent guruhlar foton bo'lmagan energiya uzatish orqali söndürücü tomonidan o'chiriladi.Peptid ko'rib chiqilayotgan fermentdan ajratilganda, etiketlash guruhi flüoresans chiqaradi.
10. Qafasli polipeptidlar
Qafasli peptidlar peptidni retseptorlari bilan bog'lanishdan himoya qiluvchi optik jihatdan olinadigan himoya guruhlariga ega.UV nurlanishiga duchor bo'lganda, peptid faollashadi va uning retseptorlari bilan yaqinligini tiklaydi.Ushbu optik faollashuv vaqt, amplituda yoki joylashuvga qarab boshqarilishi mumkinligi sababli, hujayralardagi reaktsiyalarni o'rganish uchun katak peptidlaridan foydalanish mumkin.Qafasli polipeptidlar uchun eng ko'p ishlatiladigan himoya guruhlari 2-nitrobenzil guruhlari va ularning hosilalari bo'lib, ular peptid sintezida himoya aminokislota hosilalari orqali kiritilishi mumkin.Ishlab chiqilgan aminokislota hosilalari lizin, sistein, serin va tirozindir.Biroq, aspartat va glutamat hosilalari peptid sintezi va dissotsiatsiya jarayonida sikllanishga moyilligi tufayli keng qo'llanilmaydi.
11. Poliantigen peptid (MAP)
Qisqa peptidlar odatda immunitetga ega emas va antikorlarni ishlab chiqarish uchun tashuvchi oqsillar bilan bog'lanishi kerak.Poliantigenik peptid (MAP) lizin yadrolari bilan bog'langan bir nechta bir xil peptidlardan iborat bo'lib, ular yuqori quvvatli immunogenlarni maxsus ifodalashi mumkin va peptid tashuvchisi oqsil kupletlarini tayyorlash uchun ishlatilishi mumkin.MAP polipeptidlari MAP qatronida qattiq faza sintezi orqali sintezlanishi mumkin.Biroq, to'liq bo'lmagan ulanish ba'zi filiallarda peptid zanjirlarining yo'qolishiga yoki kesilishiga olib keladi va shuning uchun asl MAP polipeptidining xususiyatlarini ko'rsatmaydi.Shu bilan bir qatorda, peptidlar alohida tayyorlanishi va tozalanishi va keyin MAP bilan birlashtirilishi mumkin.Peptid yadrosiga biriktirilgan peptidlar ketma-ketligi yaxshi aniqlangan va massa spektrometriyasi bilan osongina tavsiflanadi.
Xulosa
Peptid modifikatsiyasi peptidlarni loyihalashning muhim vositasidir.Kimyoviy modifikatsiyalangan peptidlar nafaqat yuqori biologik faollikni saqlab qolishi, balki immunogenlik va toksiklikning kamchiliklaridan samarali qochishi mumkin.Shu bilan birga, kimyoviy modifikatsiya peptidlarga yangi ajoyib xususiyatlarni berishi mumkin.So'nggi yillarda polipeptidlarni postmodifikatsiya qilish uchun CH faollashtirish usuli jadal rivojlanib, ko'plab muhim natijalarga erishildi.
Xabar vaqti: 20-mart-2023-yil
